Alkohol adalah kelompok senyawa yang mengandung satu atau lebih gugus fungsi hidroksil (-OH) pada suatu senyawa alkana. Alkohol dapat dikenali dengan rumus umumnya R-OH. Alkohol merupakan salah satu zat yang penting dalam kimia organik karena dapat diubah dari dan ke banyak tipe senyawa lainnya. Reaksi dengan alkohol akan menghasilkan 2 macam senyawa. Reaksi bisa menghasilkan senyawa yang mengandung ikatan R-O atau dapat juga menghasilkan senyawa mengandung ikatan O-H.
Salah satu senyawa alkohol, etanol (etil alkohol, atau alkohol sehari-hari), adalah salah satu senyawa yang dapat ditemukan pada minuman beralkohol. Rumus kimianya CH3CH2OH.
Contoh alkohol
Nama IUPAC
|
Nama umum
|
|
CH3CH2OH
|
Etanol
|
Etil
alkohol
|
CH3CH2CH2-OH
|
1-Propanol
|
Propil
alkohol
|
(CH3)2CH-OH
|
2-Propanol
|
Isopropil
alkohol (Catatan: bukan isopropanol)
|
2-Etil-1-butanol
|
2-Etilbutanol
|
|
3-Metil-3-pentanol
|
||
2,2-Dimetilsiklopropanol
|
||
Gugus -OH
lebih dari 1
(juga
dikenal sebagai lemak tubuh)
-OH dapat dinamai sebagai
substituen gugus hidroksil (hidroksialkana)
|
||
1,2-Etanadiol
|
Etilen
glikol
|
|
1,1-Etanadiol
|
Asetaldehid
hidrat
|
|
1,4-Sikloheksanadiol
|
||
1,2,3-Propanatriol
|
Gliserol
|
|
1,2-Di(hidroksimetil)sikloheksana
|
||
2-(hidroksimetil)-1,3-propanadiol
|
Sintesis/pembuatan alkohol





Berdasarkan
jumlah gugus fungsinya alkohol dibedakan menjadi alcohol monovalen dan alkohol
polivalen.

Ada 2 reaksi
yang dapat dipakai untuk membuat/mensintesis alkohol dari gugus karbonil:
reaksi adisi Grignard dan reaksi reduksi. Kita akan lihat satu per satu.
Reaksi adisi Grignard
Reagen
grignard dibuat dengan cara mencampurkan logam magnesium dengan alkil halida
(atau haloalkana). Atom
magnesium akan menempati posisi di antara gugus alkil dan atom halogen (X)
dengan rumus umum:
R-X + Mg →
R-Mg-X
Pada contoh
di bawah ini, digunakan bromin sebagai reagen grignard karena bromin merupakan
atom halogen yang biasa dipakai dalam pembuatan reagen grignard.
Mekanisme
dari reagen Grignard yang bereaksi dengan sebuah karbonil
Sintesis dari formaldehida
Sintesis
alkohol dari formaldehida dan reagen Grignard
Gambar
diatas menunjukkan sintesis alkohol yang dihasilkan dari formaldehida dan
reagen Grignard. Alkohol yang dihasilkan berjenis alkohol primer.
Sintesis dari aldehida
Sintesis
alkohol dari aldehida dan reagen Grignard
Gambar
diatas menunjukkan sintesis alkohol yang dihasilkan dari aldehida dan reagen
Grignard. Alkohol yang dihasilkan berjenis alkohol sekunder.
Sintesis dari keton
Sintesis
alkohol dari aldehida dan reagen Grignard
Gambar
diatas menunjukkan sintesis alkohol yang dihasilkan dari keton dan reagen
Grignard. Alkohol yang dihasilkan berjenis alkohol tersier.
Sintesis dari ester
Sintesis
alkohol dari ester dengan reduksi
Gambar
diatas menunjukkan sintesis alkohol dari ester dengan reaksi reduksi. Ester
dapat terhidrolisa menjadi alkohol dan asam karboksilat.
Sintesis dari asam karboksilat
Sintesis
alkohol dari asam karboksilat dengan reaksi reduksi
Gambar
diatas menunjukkan sintesis alkohol dari asam karboksilat dengan reaksi
reduksi.
Klasifikasi
Alkohol
Berdasarkan
jenis atom karbon yang mengikat gugus –OH, alkohol dibedakan atas alkohol
primer, alkohol sekunder, dan alkohol tersier. Dalam alkohol primer gugus –OH
terikat pada atom karbon primer, pada alkohol sekunder, gugus –OH terikat pada
atom karbon sekunder, begitu pula pada alkohol tersier, gugus –OH terikat pada
atom karbon tersier. Seperti contoh berikut:
a) Alkohol
monovalen adalah alkohol yang hanya mempunyai satu gugus fungsional –OH.
Contoh
:Etanol,Proponal
b) Alkohol
polivalen adalah jenis senyawa alkohol yang mempunyai gugus fungsional
lebih dari
satu.
Contoh|;
Etandiol ,Propantriol (gliserol)
Sifat –
Sifat Alkohol
Secara umum
senyawa alkohol mempunyai beberapat sifat, sebagai berikut :
1) Mudah
terbakar
2) Mudah
bercampur dengan air
3) Bentuk
fasa pada suhu ruang :
– dengan C 1 s/d 4 berupa gas atau cair
– dengan C 5 s/d 9 berupa cairan kental seperti minyak
– dengan C 10 atau lebih berupa zat padat
4) Pada
umumnya alkohol mempunyai titik didih yang cukup tinggi dibandingkan alkananya.Hal
ini disebabkan adanya ikatan hidrogen atas molekulnya.
Jenis-jenis Alkohol
Klasifikasi alkohol adalah sebagai berikut:
Alkohol sangat banyak peranannya untuk kehidupan manusia. Penggunaan alkohol antara lain:
Alkohol Primer
Jika gugus fungsi hidroksi terikat pada atom karbon yang hanya mengikat satu atom karbon yang lain, maka senyawa tersebut dinamakan alkohol primer. Contoh yang paling sederhana adalah etanol. Metanol bukan alkohol primer karena atom karbon yang mengikat gugus -OH tidak mengikat karbon lain.Alkohol Sekunder
Jika gugus fungsi hidroksi terikat pada atom karbon yang mengikat dua atom karbon yang lain, maka senyawa tersebut dinamakan alkohol sekunder. Contoh alkohol sekunder adalah 2-propanol.Alkohol Tersier
Jika gugus fungsi hidroksi terikat pada atom karbon yang mengikat tiga atom karbon yang lain, maka senyawa tersebut dinamakan alkoholtersier. Contoh senyawa alkohol tersier adalah 2-metil-2-propanol.Vinil Alkohol
Vinil alkohol adalah senyawa yang mempunyai gugus hidroksi yang terikat pada atom karbon berikatan rangkap dua. Contoh senyawa vinil alkohol adalah 2-propenol.Benzil Alkohol
Benzil alkohol adalah senyawa yang mempunyai gugus hidroksi yang terikat pada gugus benzil. Gugus benzil mempunyai rumus C6H5-CH2-.Alkohol Dihidrat
Alkohol dihidrat adalah senyawa yang mengandung dua gugus hidroksi. Contoh alkohol dihidrat adalah etilen glikol.Alkohol Trihidrat
Alkohol triidrat adalah senyawa yang mengandung tiga gugus hidroksi. Contoh alkohol trihidrat adalah gliserol.Manfaat Alkohol
Alkohol sangat banyak peranannya untuk kehidupan manusia. Penggunaan alkohol antara lain:
- Etanol digunakan sebagai bahan antiseptik, pelarut parfum, bahan bakar, dan campuran minuman keras.
- Campuran antara metanol dan metilen biru membentuk spiritus untuk bahan bakar.
- Dapat digunakan untuk pengawetan di bidang medis (selain formalin).
- Alkohol merupakan pelarut yang sangat baik.
- Etilen glikol bermanfaat untuk pembuatan lem serbaguna.
FENOL 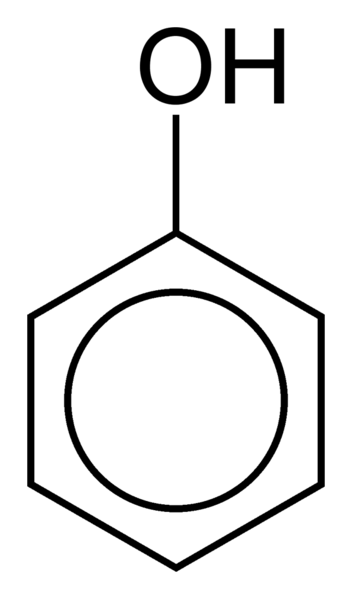

Fenol atau asam karbolat atau benzenol adalah zat kristal tak berwarna yang memiliki bau khas. Rumus kimianya adalah C6H5OH dan strukturnya memiliki gugus hidroksil (-OH) yang berikatan dengan cincin fenil.
Fenol (ArOH) ialah senyawa
dengan suatu gugus OH yang terikat pada cincin aromatic. Gugus OH merupakan
activator kuat dalam reaksi substitusi aromatic elektrofilik. Karena ikatan sp2
lebih kuat dari pada ikatan oleh karbon sp3, maka ikatan C-O dari
suatu fenol tidak mudah terputuskan. Meskipun ikatan C-O fenol tidak mudah
patah, ikatan OH mudah putus. Fenol reaksi lainya yang menarik adalah reaksi
dengan kloroform dalam basa berair yang disusul dengan perlakuan dengan asam
berair.
Fenol adalah suatu gugus senyawa yang dianggap berasal
dari benzene dengan mengganti satu atau lebih atom H dengan gugus ori atau
hidroksil. Oleh karena itu fenol dapat dibedakan atas fenol monovalen, bila
hanya satu atom H diganti dengan gugus OH. Fenol divalent, bila 2 atom H. fenol
bersifat sebagai asam lemah didalam air. Karena mengalami ionisasi, fenol dapat
digunakan sebagai anti septic, pembuatan asam fikrat, asam solosilat, dan
lain-lain (Margen, 1982).
Suatu
fenol adalah suatu senyawa dengan suatu gugus OH yang
terikat pada cincin aromatic elektronik, meskipun ikatan C-O fenol tidak mudah
pecah, ikatan OH mudah putus. Fenol merupakan asam yang lebih kuat dari alcohol
dan air. Fenol sendiri bertahan terhadap oksidasi, karena pembentukan suatu
gugus karbonil akan mengakibatkan dikarbonya penstabilan aromatik (Fessenden,
1982).
Gugus hidroksil adalah gugus pengaktif yang kuat
sehingga fenol akan mengalami reaksi substitusi elektronik pada kondisi yang
rusak sekalipun. Misalnya fenol dapat dinitrasi dengan memperlakukannya dengan
asam nitrat encer dan akan memberikan paling banyak isomer nitrofenol (Siregar,
1988).
Permasalahan :
Kita tahu bahwa Alkohol dan Fenol memiliki gugus -OH. Bagaimana mekanisme reaksi pembuatan Fenol dan Alkohol?


Nama : Wulandari
BalasHapusNIM : A1C112006
Baiklah saya akan mencoba menjawab permasalahan saudara Daniel.
Alkohol dapat dibuat dengan mereaksikan antara alkil halida dengan suatu basa. Selain itu juga diperoleh produk lain, yakni garam halide
CH3-CH2-Cl + KOH -----> CH3-CH2-OH + KCl
Sedangkan fenol dapat dihasilkan dengan metode cumene. Metode cumene terdiri dari tiga tahap sintesis:
(1) Alkilasi benzena menjadi cumene (isopropil benzene)
(2) Oksidasi cumene menjadi cumene hidroperoksida
(3) Dekomposisi hidroperoksida menjadi fenol dan aseton.
Metode ini memiliki kelebihan yaitu membutuhkan material awal yang murah berupa benzena dan propilen dan diubah menjadi dua produk bernilai tinggi berupa fenol dan aseton.
Proses produksi fenol dengan metode cumene memiliki beberapa kelemahan seperti dihasilkannya intermediet yang eksplosif berupa cumene hidroperoksida sehingga berbahaya bagi lingkungan
Sekian semoga dapat membantu :)
Baiklah, saya akan mencoba menjawab permasalahan saudara.
BalasHapusAlkohol dapat dibuat melalui Hidrolisis Ester.
Rumus ester suatu asam organik adalah RCOOR'. Bila ester tersebut dihidrolisis dapat menghasilkan alkohol dan asam karboksilat menurut persamaan reaksi:
RCOOR' + H2O ⇌ RCOOH + R'OH
Fenol merupakan bahan kimia industri yang sangat penting, sebagai material awal untuk sejumlah besar produk komersial mulai dari aspirin sampai plastik.
Fenol dapat dibuat melalui Hidrolisis Klorobenzena (Proses Dow)
Sebenarnya ada gambar nya, berhubung dikolom komentar tidak bisa. Nanti akan saya jelaskan kepada saudara.
Nama : Ekin Dwi Arif k (A1C112011)
BalasHapusDari apa yang saya dapat dari literatur bahwa
Fenol merupakan bahan kimia industri yang sangat penting, sebagai material awal untuk sejumlah besar produk komersial mulai dari aspirin sampai plastik. Hidrolisis Klorobenzena (Proses Dow)
berhubung gambarnya tidak bisa ditampilkan. maka saya menjelaskannya nanti
pembuatan alkohol dengan : Hidrasi Alkena Adisi air pada ikatan rangkap alkena dengan katalis asam. Metode pembuatan alkohol dengan berat molekul rendah (kegunaan utama pada proses industri skala besar). Katalis asam yg paling sering digunakan: asam sulfat & asam fosfat.
sebenarnya ada gambar yang ingin tampilkan tetapi tidak bisa. jadi saya akan menjelaskannya nanti