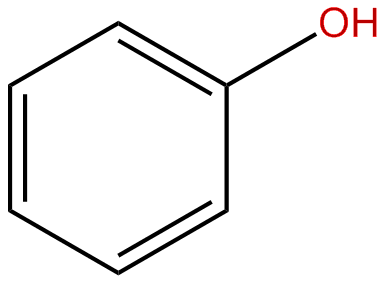
Fenol (fenil alcohol) merupakan zat padat yang tidak berwarna yang mudah meleleh dan terlarut baik didalam air. Dalam mencoba keasaman reaksi dalam zat-zat kimia seperti asam asetat, dan lain-lain banyak digunakan indicator, indicator seperti kertas lakmus.
Fenol
yang diketahui fungsinya sebagai zat desinfektan yang umum dipakai
orang. Berbeda dengan alcohol alifatik, fenol sebagai alkohol aromatik
mempunyai sifat yang berbeda. Dalam air fenol sedikit terionisasi
menghasilkan ion H+ dengan Ka = 10-10.
Suatu
fenol (ArOH) ialah senyawa dengan suatu gugus OH yang terikat pada
cincin aromatic. Gugus OH merupakan activator kuat dalam reaksi
substitusi aromatic elektrofilik. Karena ikatan sp2 lebih kuat dari pada ikatan oleh karbon sp3,
maka ikatan C-O dari suatu fenol tidak mudah terputuskan. Meskipun
ikatan C-O fenol tidak mudah patah, ikatan OH mudah putus. Fenol reaksi
lainya yang menarik adalah reaksi dengan kloroform dalam basa berair
yang disusul dengan perlakuan dengan asam berair.
Fenol
adalah suatu gugus senyawa yang dianggap berasal dari benzene dengan
mengganti satu atau lebih atom H dengan gugus ori atau hidroksil. Oleh
karena itu fenol dapat dibedakan atas fenol monovalen, bila hanya satu
atom H diganti dengan gugus OH. Fenol divalent, bila 2 atom H. fenol
bersifat sebagai asam lemah didalam air. Karena mengalami ionisasi,
fenol dapat digunakan sebagai anti septic, pembuatan asam fikrat, asam
solosilat, dan lain-lain (Margen, 1982).
Suatu fenol
adalah suatu senyawa dengan suatu gugus OH yang terikat pada cincin
aromatic elektronik, meskipun ikatan C-O fenol tidak mudah pecah, ikatan
OH mudah putus. Fenol merupakan asam yang lebih kuat dari alcohol dan
air. Fenol sendiri bertahan terhadap oksidasi, karena pembentukan suatu
gugus karbonil akan mengakibatkan dikarbonya penstabilan aromatik (Fessenden, 1982).
Gugus
hidroksil adalah gugus pengaktif yang kuat sehingga fenol akan
mengalami reaksi substitusi elektronik pada kondisi yang rusak
sekalipun. Misalnya fenol dapat dinitrasi dengan memperlakukannya dengan
asam nitrat encer dan akan memberikan paling banyak isomer nitrofenol
(Siregar, 1988).
Kelarutan
Fenol memiliki kelarutan terbatas dalam air, yakni 8,3 gram/100 ml. Fenol memiliki sifat yang cenderung asam, artinya ia dapat melepaskan ion H+ dari gugus hidroksilnya. Pengeluaran ion tersebut menjadikan anion fenoksida C6H5O− yang dapat dilarutkan dalam air.
Dibandingkan dengan alkohol alifatik lainnya, fenol bersifat lebih asam. Hal ini dibuktikan dengan mereaksikan fenol dengan NaOH, di mana fenol dapat melepaskan H+. Pada keadaan yang sama, alkohol alifatik lainnya tidak dapat bereaksi seperti itu. Pelepasan ini diakibatkan pelengkapan orbital antara satu-satunya pasangan oksigen dan sistem aromatik, yang mendelokalisasi beban negatif melalui cincin tersebut dan menstabilkan anionnya.
Permasalahan :
Kelarutan
Fenol memiliki kelarutan terbatas dalam air, yakni 8,3 gram/100 ml. Fenol memiliki sifat yang cenderung asam, artinya ia dapat melepaskan ion H+ dari gugus hidroksilnya. Pengeluaran ion tersebut menjadikan anion fenoksida C6H5O− yang dapat dilarutkan dalam air.
Dibandingkan dengan alkohol alifatik lainnya, fenol bersifat lebih asam. Hal ini dibuktikan dengan mereaksikan fenol dengan NaOH, di mana fenol dapat melepaskan H+. Pada keadaan yang sama, alkohol alifatik lainnya tidak dapat bereaksi seperti itu. Pelepasan ini diakibatkan pelengkapan orbital antara satu-satunya pasangan oksigen dan sistem aromatik, yang mendelokalisasi beban negatif melalui cincin tersebut dan menstabilkan anionnya.
Permasalahan :
Bagaimana cara membuat Fenol dan apakah yang membedakan alcohol
dengan fenol selain dari strukturnya fenolnya yang memiliki rangkaian
siklik/tertutup/aromatik?
Fenol didapatkan melalui oksidasi sebagian pada benzena atau asam benzoat dengan proses Raschig, Fenol juga dapat diperoleh sebagai hasil dari oksidasi batu bara.
BalasHapusuntuk membedakan fenol dan alkohol dapat dilihat dari wujudnya, dimana fenol berbentuk kristal tak berwarna dan berbau khas, sedangkan alkohol berwujud cair. selain itu, kita dapat membedakan dari sifat fisik dan kimianya. dimana alkohol dgn atom C bersuku rendah dapat larut dalam air, sedangkan pada fenol kelarutan dalam air terbatas, fenol juga tidak dapat dioksidasi menjadi aldehid atau keton sedangkan alkohol dapat dioksidasi menjadi aldehid atau keton, fenol juga dapat digunakan sebagai antiseptik namun fenol terkonsentrasi dapat mengakibatkan pembakaran kimiawi pada kulit yang terbuka.
Oke trimakasih saudari astri
BalasHapusNama : Ekin Dwi Arif
BalasHapusNim: A1C112011
Untuk membuat fenol dapat ditempuh empat macam cara, yaitu: (a) meleburkan garam Na-arilsulfonat dan NaOH, (b) menghidrolisis garam diazonium, (c) melalui proses Dow, dan (d) mengoksidasi kumena. Cara yang lazim dilakukan untuk membuat fenol dalam industri dewasa ini adalah oksidasi kumena.
Alkohol dan fenol adalah senyawa yang sama-sama mengandung gugus OH.
Perbedaannya:
1. Alkohol memiliki rantai karbon terbuka, fenol memiliki rantai karbon tertutup/melingkar.
2. Alkohol dan fenol bersifat asam lemah. Namun, sifat asam pada fenol lebih kuat daripada alkohol karena fenol memiliki anion dengan muatan negatif yang disebar oleh cincin karbon melingkar. Alkohol adalah asam yang sangat sangat sangat lemah, hampir netral.
3. Alkohol tidak bereaksi dengan basa (karena sifatnya yang sangat lemah), sedangkan fenol bereaksi dengan basa.
4. Alkohol bereaksi dengan Na atau PX3, sedangkan fenol tidak bereaksi. (X adalah halogen)
5. Alkohol bereaksi dengan asam karboksilat, sedangkan fenol tidak.
oke trimakasi saudara Ekin
BalasHapusUntuk membuat fenol dapat ditempuh empat macam cara, yaitu: (a) meleburkan garam Na-arilsulfonat dan NaOH, (b) menghidrolisis garam diazonium, (c) melalui proses Dow, dan (d) mengoksidasi kumena. Cara yang lazim dilakukan untuk membuat fenol dalam industri dewasa ini adalah oksidasi kumena.
BalasHapusuntuk membedakan fenol dan alkohol dapat dilihat dari wujudnya, dimana fenol berbentuk kristal tak berwarna dan berbau khas, sedangkan alkohol berwujud cair. selain itu, kita dapat membedakan dari sifat fisik dan kimianya. dimana alkohol dgn atom C bersuku rendah dapat larut dalam air, sedangkan pada fenol kelarutan dalam air terbatas, fenol juga tidak dapat dioksidasi menjadi aldehid atau keton sedangkan alkohol dapat dioksidasi menjadi aldehid atau keton, fenol juga dapat digunakan sebagai antiseptik namun fenol terkonsentrasi dapat mengakibatkan pembakaran kimiawi pada kulit yang terbuka.
Terimakasih banyak saudari ema Sudah membantu :D
BalasHapus